Oborové aktuality – Internista
Rizika polypragmazie u kardiologického pacienta
18. 6. 2024 - redPřehled přednášek (kliknutím na odkaz se dostanete rovnou k dané přednášce):
- Proč lékové interakce v kardiologii? (Jiří Vítovec)
- Nebezpečí polypragmazie s ohledem na lékové interakce perorálních antikoagulancií (Jiří Slíva)
- Praktické aspekty antikoagulační léčby – význam monitorace (Tomáš Kvasnička)
Proč lékové interakce v kardiologii?
prof. MUDr. Jiří Vítovec, CSc., FESC, 1. interní kardioangiologická klinika LF MU FN u sv. Anny, Brno
S přibývajícími novými léky je třeba se stále více zamýšlet nad problematikou lékových interakcí a polypragmazie. Základními typy lékových interakcí jsou interakce farmaceutické, kdy léčiva podávaná najednou nejsou chemicky nebo fyzikálně kompatibilní, farmakokinetické, tedy absorpce, distribuce, transformace, metabolismus a eliminace, a farmakodynamické, při nichž dochází ke změnám účinku na úrovni receptorů nebo společným působením na stejný fyziologický systém.
Lék je při průchodu gastrointestinálním traktem ovlivněn cytochromem P450 a P-glykoproteinem. Nejrozšířenější formou cytochromů P450 je CYP3A4, který se podílí na většině známých přeměn léčiv, jež probíhají za účasti cytochromů P450. Lékové interakce na úrovni CYP3A4 jsou způsobeny jak indukcí tohoto enzymu, tak jeho inhibicí. Substrátem CYP3A4 je například amiodaron, jehož inhibitorem je cyklosporin a induktorem dexametazon. Dalším příkladem substrátu CYP3A4 je atorvastatin, který je inhibován grapefruitovým džusem. Warfarin je substrátem CYP2C9 a jeho induktorem je třezalka. Problém s třezalkou byl asi před 15 lety popsán v časopise Lancet, kdy pacientka po transplantaci ledvin užívala cyklosporin a dařilo se jí dobře. Na kontrolu však přišla s projevy selhání štěpu, což bylo způsobeno tím, že cyklosporin zapíjela třezalkou a byla v podstatě předávkována.
Dalším produktem, který ovlivňuje metabolismus léku, je P-glykoprotein. Řadí se mezi nejvýznamnější eliminační glykoproteiny. Tímto substrátem je ovlivněna asi polovina léků. Pracuje ve spolupráci s „detoxikačními“ enzymy systému CYP (zejména CYP3A4), působí v enterocytech, hepatocytech, proximálních tubulech a endotelu. Tento glykoprotein inhibuje nebo aktivuje řada léků nebo složek potravy.
Farmakodynamických interakcí je mnoho. Příklady kombinací léků a jejich efekt:
- betablokátor + verapamil: bradykardie a pokles inotropie
- betablokátor + digoxin: bradykardie
- antitrombotika + nesteroidní antiflogistika (NSAID): krvácení
- inhibitory angiotenzin konvertujícího enzymu/blokátory receptorů pro angiotenzin II (ACEi/ARB) + NSAID: zvýšení krevního tlaku, zhoršení funkce levé komory
- léky prodlužující interval QT + diuretika: arytmie
- ACEi/ARB + suplementace kalia: hyperkalemie
- inhibitory PDE5 (inhibitory fosfodiesterázy typu 5) + nitroglycerin: hypotenze
Dnes existuje řada webových stránek lékových interakcí, kde lze vyhledávat. Patří mezi ně i rubrika „Z farmakologie“ na webu www.kapitolyonline.cz.
Závažným problémem je v současné době polypragmazie, která je spojena nejen se snížením adherence, ale i s častější hospitalizací a vyšší mortalitou. Podíváme-li se z tohoto úhlu pohledu na syndrom srdečního selhání, vidíme, že je zde přítomna celá řada komorbidit. Každá komorbidita vede k nějaké farmakoterapii a ve výsledku užívá pacient řadu léků, které nemusejí mít prokázanou účinnost, pacient tyto léky nepotřebuje, mohou mu škodit a v konečném důsledku mají léčit nežádoucí účinky jiných léků. Tyto léky pacient užívá 3krát denně, přičemž existují retardované formy. Čím více léků, tím větší je riziko nežádoucích účinků, farmakologických interakcí a omylů při užívání léků a horší adherence k léčbě. Polypragmazie samozřejmě také zvyšuje náklady na léčbu. Držme se tedy citátu J. E. Purkyně: „Aby léčba nebyla horší než nemoc sama.“
Nebezpečí polypragmazie s ohledem na lékové interakce perorálních antikoagulancií
doc. MUDr. Jiří Slíva, Ph.D., Ústav farmakologie 3. LF UK, Praha
Polypragmazie je záležitost velmi aktuální. Svědčí o tom třeba data, která ukazují, že zhruba třetina seniorů, kteří jsou léčeni na interních odděleních, je hospitalizována z důvodu nežádoucích účinků, případně lékových interakcí. To je číslo opravdu zarážející a alarmující. Máme mnohé možnosti, jak to zlepšit, ale řada možností je mimo naši kontrolu. Například to, že si pacienti nakupují různá léčiva a doplňky stravy, o jejichž interakcích nemají ani tušení.
Polypragmazie v kardiologii je spojena s rizikem nežádoucích účinků, s non-adherencí, negativního dopadu na kvalitu života a samozřejmě i s rizikem lékových interakcí. Autoři Huang a kol. (2010) hodnotili ve své studii souvislost mezi počtem předepsaných léků a rizikem pádů v populaci diabetiků 2. typu. Tito pacienti pro své mikrovaskulární a kardiovaskulární komplikace užívají celou škálu medikamentů. Ve studii bylo zjištěno, že pacienti užívající čtyři a více léků mají zvýšené riziko pádů, což pro starší pacienty představuje život ohrožující stav.
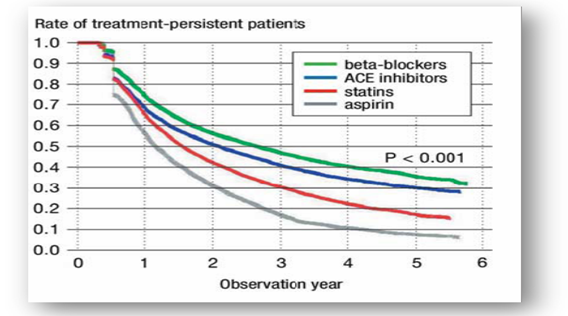
Non-adherence je celosvětový problém a téma, které se táhne jako červená nit napříč všemi obory medicíny. A obecně platí, co nás nebolí, to nás netrápí. Dyslipidemie nebo vysoká hodnota LDL cholesterolu opravdu nebolí a pacienti si jen velmi těžko připouštějí, že se musejí léčit. Nejsou ochotni léky užívat dlouhodobě a pravidelně, což představuje velké riziko. Studie autorů Mangiapane a kol. (2011) sledovala adherenci a perzistenci u více než 30 tisíc pacientů po infarktu myokardu. V průběhu let adherence k léčbě betablokátory, ACEi, statiny a aspirinem významně klesala.
Chronická nemoc má nejen v kardiologii vliv na kvalitu života. Pokud je ale nemocný dále zatížen polypragmazií, je jeho kvalita života ještě horší, a to v aspektech, jako je soběstačnost, běžné denní aktivity, mobilita a další.
Polypragmazie je alfou-omegou lékových interakcí. Ty ale nejsou jenom špatné, vždyť bez nich bychom tady neměli ty úžasné dvoj- a trojkombinace léčiv. Farmakokinetické lékové interakce jsou nejčastěji přičítány cytochromu P450, který má řadu izoforem, kde můžeme působit indukčně nebo inhibičně. Nicméně tento typ lékových interakcí probíhá na všech úrovních farmakokinetiky, což je absorpce, distribuce a exkrece, přičemž pro nás nejdůležitější je biotransformace.
Třetina až polovina známých léčiv je metabolizována systémy CYP3A4 a CYP2C9, ale tento podíl se stále zmenšuje. Je to proto, že se používá stále více biologik nebo obecných přípravků, které nejsou substrátem, nejsou tedy metabolizovány mikrozomálním systémem.
Nejčastěji užívané léčivé látky s potenciálem lékových interakcí v populaci seniorů uvádí studie z roku 2021 (Hughes et al.). Na prvním místě je warfarin, na třetím atorvastatin a na pátém místě je furosemid. Jsou to všechno léky, které se hojně předepisují.
Podívejme se na perorální antikoagulancia, tedy warfarin, a přímá perorální antikoagulancia (DOAC), tedy dabigatran, apixaban, edoxaban a rivaroxaban. DOAC se mezi sebou odlišují v mnoha parametrech a liší se i od warfarinu. Warfarin má nejdelší biologický poločas (cca 2 dny), nejdelší dobu do dosažení maximální plazmatické hladiny (3–5 dní) a jednoznačně nejvíce lékových interakcí. Warfarin je polymorfně metabolizován, z velké části se váže na bílkoviny krevní plazmy, ať už je to albumin, nebo alfa-1-glykoprotein. Na úrovni alfa-1-glykoproteinu je řada chromatograficky odlišitelných variant, které „mají warfarin více či méně rády“. Když si toto uvědomíme, tak tím v podstatě určujeme velikost volné frakce warfarinu a čím je tato frakce vyšší, tím vyšší je jeho účinek. Dále jsou zde polymorfismy na úrovni P-glykoproteinu, které určují, jak bude látka prostupovat přes buněčné membrány. Warfarin může mít jak farmakokinetické, tak i farmakodynamické vlastnosti. Jistě je nám všem známo, že warfarin se nemá kombinovat s listovou zeleninou, protože ta obsahuje vitamin K. Totéž platí také pro zelený čaj a různé doplňky stravy (chlorella). Na tvorbě vitaminu K participuje mikrobiota, kterou mohou ovlivňovat různá antibiotika.
Z farmakokinetických interakcí bych zmínil distribuci, a to jednak na úrovni genetické výbavy, ale i v případě menší nabídky albuminu nebo alfa-1-glykoproteinu v důsledku albuminurie nebo nižší syntézy albuminu, kdy bude vzrůstat volná frakce warfarinu a zvyšovat se jeho účinnost. Možné interakce jsou na úrovni vzájemné kompetice o bílkoviny, na úrovni CYP2C9, který je klíčový pro metabolismus S-warfarinu, ale jsou to i další varianty, CYP1A2 nebo CYP3A4, a těch možných induktorů nebo naopak inhibitorů je nepřeberně.
Farmakodynamické lékové interakce DOAC jsou dobře predikovatelné a jsou velmi podobné lékovým interakcím u warfarinu, s výjimkou interakcí na úrovni vitaminu K. Literárně je zmiňováno také možné vyšší riziko krvácení v kombinaci s antidepresivy nebo anxiolytiky ze skupiny SSRI/SNRI, pravděpodobně za to může větší nabídka serotoninu, ale klinická relevance je diskutabilní.
Rizika jsou zjevná, žádný lék není zcela prost nežádoucích účinků ani lékových interakcí. Nicméně z pohledu lékových interakcí jsou rizika spojená s užíváním DOAC o poznání menší v porovnání s warfarinem.
Praktické aspekty antikoagulační léčby – význam monitorace
doc. MUDr. Tomáš Kvasnička, CSc., Trombotické centrum ÚLBLD, VFN a 1. LF UK, Praha
Antikoagulancia, která dnes v klinické praxi používáme, zasahují do koagulační kaskády různými mechanismy a liší se i v jiných parametrech. Zástupci parenterálních přípravků jsou nefrakcionovaný heparin, nízkomolekulární hepariny a fondaparinux, mezi perorální přípravky pak patří warfarin (antagonista vitaminu K) a přímá perorální antikoagulancia (DOAC) – dabigatran, rivaroxaban, apixaban a edoxaban.
Přes některé výhody má tradiční antikoagulační terapie warfarinem i své nevýhody: vyžaduje pravidelnou monitoraci INR (mezinárodní normalizovaný poměr), dávkovací spektrum je velmi široké, hodnota INR kolísá v závislosti na řadě okolností, zvláště v důsledku četných lékových interakcí. Účinnost a bezpečnost ovlivňují zevní vlivy i vrozené predispozice. Nicméně z hlediska koagulační léčby má warfarin nejširší indikace. Hepariny a nízkomolekulární hepariny (LMWH) jsou nepřímá parenterální antikoagulancia. Jejich účinek je zprostředkován plazmatickými kofaktory, nemají tedy vlastní vnitřní antikoagulační aktivitu. Dnes jsou v převážné většině užívány jak v prevenci, tak v léčbě tromboembolické nemoci LMWH, hlavně pro svůj lepší farmakokinetický profil a předvídatelnost účinku. Jejich nevýhodou je parenterální aplikace, což s sebou nese zvýšené riziko vzniku hematomů. Účinek LMWH není, až na výjimky, nutné monitorovat. Laboratorní kontrola účinnosti je vhodná zejména u pacientů s indexem tělesné hmotnosti (BMI) > 40, s renální insuficiencí a u gravidních pacientek, onkologických pacientů a dětí.
Jako poslední byla do praxe zavedena DOAC. Dabigatran, přímý inhibitor trombinu, je zástupcem skupiny gatranů. Do skupiny xabanů patří rivaroxaban, apixaban a edoxaban, tedy inhibitory faktoru Xa. Výhodou DOAC je perorální užití, rychlý nástup i odeznění účinku a předvídatelné působení umožňující fixní dávkování bez nutnosti laboratorní monitorace. DOAC mají také výrazně menší riziko lékových interakcí než warfarin. Většina indikací DOAC se týká prevence, pouze jedna indikace je léčebná. S tím pak souvisejí i podmínky úhrad, které stanovuje Státní ústav pro kontrolu léčiv. Na jednotlivé indikace reflektuje i dávkování, které je striktně vymezeno, s výjimkou některých omezení, jako je snížená hmotnost, originální parametry, možná koincidence dalších nezbytně nutných medikamentů.
Kardiovaskulární onemocnění, zejména ischemická choroba srdeční (ICHS), jejich léčba, primární i sekundární prevence jsou stále diskutovaným tématem. Jednou z nejlepších studií v této oblasti byla studie COMPASS, která prokázala účinnost užití rivaroxabanu spolu s kyselinou acetylsalicylovou (ASA) v rámci sekundární prevence u pacientů trpících ICHS nebo ICHDK (ischemická choroba dolních končetin), tzv. vaskulární prevence. Studie byla předčasně ukončena vzhledem k výrazné účinnosti v rameni s rivaroxabanem 2,5 mg 2× denně (vaskulární dávka) + ASA 100 mg 1× denně.
Úskalí antikoagulační léčby v klinické praxi souvisí s tím, že se jedná o léčbu s potenciálním rizikem krvácení. To má samozřejmě i forenzní rizika pro ošetřujícího lékaře, a proto bych rád zdůraznil, že je vždy třeba brát na zřetel SPC každého přípravku a striktně dodržovat uvedené pokyny.
Pacienti, kteří jsou DOAC léčeni, mají k dispozici i edukační materiály, v nichž jsou mimo jiné uvedeny veškeré potřebné informace o příslušném léku a zejména pak kontakty na lékaře pro případ, že by došlo k nějaké naléhavé komplikaci léčby.
Riziko krvácení existuje pochopitelně i u LMWH, například při samoaplikaci může dojít k podání nesprávné dávky, což může vést k ovlivnění účinku. Při této léčbě je také nutno hodnotit hematomy v místě vpichu a eventuální projevy alergií. Vzhledem k riziku heparinem indukované trombocytopenie (HIT) se mají po 5–10 dnech po zavedení terapie s LMWH kontrolovat hodnoty trombocytů. V graviditě je třeba podávat pouze preventivní dávky LMWH. Obezřetnosti je třeba u gravidních pacientek s anamnézou trombózy nebo s Leidenskou mutací, u kterých se v 15. týdnu gravidity zjistí vyšší riziko preeklampsie. Gynekologové těmto pacientkám okamžitě nasadí 150 mg acetylsalicylátu, což v kombinaci s profylaxí LMWH vede k tvorbě obrovských hematomů.
O úskalí léčby warfarinem bylo již mnohé řečeno. Důležitá jsou zde režimová opatření, strava, pravidelné kontroly INR a v neposlední řadě snaha o snižování rizika krvácivých komplikací, například eliminace nevhodných sportovních aktivit.
Při léčbě DOAC je třeba dbát na správné dávkování a pravidelné užívání (u rivaroxabanu s jídlem). Nutností jsou pravidelné kontroly renálních parametrů, včetně včasné kontroly u fragilních pacientů a při zvýšeném riziku dehydratace, a dle hodnot clearance kreatininu ev. redukce dávkování.
Je obecně známo, že léčba DOAC se rutinně monitorovat nemusí, může ale nastat celá řada situací, kdy je vhodné, respektive nutné tuto léčbu laboratorně zhodnotit. Je to ale problém. Sofistikovanou metodou pro určení plazmatických koncentrací všech DOAC je kapalinová chromatografie, nicméně tato metoda je zcela nedostupná. Rutinní koagulační screeningové testy nejsou vhodné. Používají se kvantitativní (minimální-maximální koncentrace) kalibrované chromogenní testy, z nichž lze získat obrovské množství dat a je vidět, že to nějakým způsobem funguje. Jak exaktně, tedy to, co bychom chtěli vědět, nám tyto testy zatím neumožňují zjistit.
Bezpečnost antikoagulační léčby DOAC se zvyšuje s možností použití specifických antidot v případě krvácení nebo k eliminaci antikoagulačního účinku v případě neodkladné operace apod. K dispozici je antidotum dabigatranu – přípravek Praxbind (idarucizumab), který je u dospělých pacientů indikován v situacích, kdy je třeba urychleně zvrátit antikoagulační účinky při naléhavých chirurgických nebo jiných urgentních výkonech nebo při život ohrožujícím nebo nekontrolovaném krvácení. K reverzi účinku rivaroxabanu a apixabanu je k dispozici přípravek Ondexxya (andexanet alfa), který je v nízké nebo vysoké dávce indikován při život ohrožujícím nebo nekontrolovaném krvácení. Cena přípravku je ovšem ohromující – nízká dávka stojí 250 tisíc korun a vysoká dávka pak 450 tisíc korun.
Monitorace antikoagulačně působících přípravků:
VKA: nutnost stanovení INR (titrace dávkování je individuální)
LMWH: stanovení hodnot antiXa (pouze vyhraněné případy)
DOAC: predikovatelný farmakokinetický a farmakodynamický profil -> rutinní monitorace není nutná
! Rychlá reverze účinku (antidota: dabigatran etexilát, rivaroxaban, apixaban)
 Ilustrační fotografie. Zdroj: iStock
Ilustrační fotografie. Zdroj: iStock



