Monoklonální protilátky a inhibující oligonukleotidy – téma stále aktuálnější
Souhrn
Moderní farmakologie přináší řadu nových terapeutických přístupů. Ke klasickým „malým“ molekulám se již před více než desetiletím přidala „biologická“ léčba s použitím cíleně působících monoklonálních protilátek a v posledních letech přichází další slibná skupina, jakou jsou inhibující oligonukleotidy, fragmenty a analoga ribonukleové kyseliny (mikroRNA). Léčba monoklonálními protilátkami náleží především do rukou specialistů, nicméně setkávají se s nimi i praktičtí lékaři. Hlavní doménou využití monoklonálních protilátek v léčbě je onkologie, revmatologie, gastroenterologie či infektologie. Postupně se však jejich využití rozšiřuje na další obory, zejména na kardiologii. Příkladem je zavedení dvou nových skupin léčiv: inhibitorů proproteinové konvertázy subtilisin/kexinového typu 9 (hypolipidemika alirocumab či evolocumab) nebo antidota proti dabigatranu – přímému inhibitoru trombinu (idarucizumab). Naopak léčba inhibujícími oligonukleotidy se užívá při onkologických či metabolických onemocněních zatím sporadicky. Nicméně v mnoha indikacích je řada oligonukleotidů v pokročilé fázi klinického hodnocení, a tak lze očekávat nástup i tohoto vysoce specifického typu léčby. Oběma léčebným postupům je společné mnoho vlastností, dominuje však velmi vysoká specificita léčby cílená na jednu konkrétní molekulu či strukturu. Dále to je nutnost parenterální aplikace, dlouhá až velmi dlouhá doba působení, vyšší náklady či absence lékových interakcí na bázi farmakokinetiky. Rozdílný je však mechanismus účinku, monoklonální protilátky vyváží již přítomnou molekulu v cirkulaci, naopak inhibující oligonukleotidy zamezí její tvorbě na úrovni translace a transkripce genu. (Kap Kardiol 2020; 12: 12–17)
Klíčová slova
· biologická léčba · monoklonální protilátky · inhibující oligonukleotidy · mikroRNA · onkologie · revmatologie · metabolické choroby · kardiologie
Úvod
Za prudký rozvoj farmakologie a za významné pokroky v léčbě onkologických, gastroenterologických, revmatologických a v neposlední řadě i kardiologických nemocných vděčíme novým léčebným postupům cíleným na jednu konkrétní molekulu. Většina strategií je zaměřena na zamezení účinku. Toho docilujeme buď přísně zacílenou inhibicí syntézy již na úrovni genu, či specifickým vyvázáním molekuly v plazmě blokujícím její efekt. Přesnost zacílení léčby umožnily poznatky z oblasti molekulární biologie, které přinesly detailní znalost patologických dějů (zpravidla vyřazením funkce konkrétního genu). Další inspirací byla analýza genetických odchylek (jak se sníženou aktivitou, tedy mutací loss‑of‑function, či naopak s aktivitou vyšší, tedy mutací gain‑of‑function). Analýza těchto vztahů umožnila dnešní skutečně „molekulární“ přístup k léčbě s vyřazením či se zamezením tvorby konkrétní molekuly. Současná mikromolekulární léčiva, tedy chemické látky, mají specificitu významně menší. Příkladem jsou např. inhibitory angiotenzin‑konvertujícího enzymu, které vedle blokády konverze angiotenzinu I na účinný angiotenzin II blokují též degradaci řady působků, např. bradykininu či neuropeptidů. Jiným je antivitamin K – warfarin, který inhibuje nejen syntézu některých „vitamin K‑dependentních“ koagulačních faktorů, ale i dalších pochodů vyžadujících redukovaný vitamin K, např. metabolismus kolagenu.
Přesné cílení na konkrétní molekulu s úkolem vyřadit její funkci dosud umožnily a stále umožňují specifické monoklonální protilátky. V současné době užíváme více než 500 různých monoklonálních protilátek a každým rokem jich několik desítek přibývá. Proto je tento článek zaměřen především na ně. Druhou, novější strategií je omezení syntézy dané molekuly vyřazením příslušného genu. Zde se uplatňují zejména oligonukleotidy (nazývané microRNA – miRNA), tedy řetězce 20–25 nukleotidů nekódujících RNA, které regulují expresi cílového genu a syntézu daného proteinu. K terapeutickým účelům se užívají především analoga přirozených miRNA, která jsou chráněna před degradací. Jelikož i tato oblast farmakoterapie je v explozivním rozvoji, je vhodné krátce se zmínit i o ní.
Monoklonální protilátky – biologická léčba
Použití protilátek v medicíně má sice dlouholetou tradici – před 125 lety byl užit k léčbě difterický anatoxin –, nicméně na dnešní rozkvět jsme si museli celé století počkat. Prvá monoklonální protilátka (mAb) – muromonab‑CD3 – byla schválena ke klinickému použití u akutní rejekce transplantátu ledvin či srdce až v roce 1986. Cesta, která vedla k zavedení monoklonálních protilátek do praxe, byla lemována hned čtyřmi Nobelovými cenami. Za využití tetanového a difterického antitoxinu byl počátkem 20. století odměněn cenou Emil Adolf von Behring a brzy po něm byla medaile udělena Paulu Ehrlichovi za „teorii postranních řetězců” pro interakci protilátky s antigenem a formulování teorie „zámku a klíče“. O půlstoletí později pak cenu obdržel Linus Pauling za potvrzení této teorie. Poslední Nobelovu cenu pak získali v roce 1986 César Milstein a Georges Köhler za vývoj metody pro výrobu „vlastních“ monoklonálních protilátek. Cesta k nové epoše tím byla otevřena.
1. Princip a cíle léčby na podkladě monoklonálních protilátek
Proč je biologická léčba na bázi monoklonálních protilátek v popředí zájmu farmakologů, kliniků i farmaceutických firem? Důvod je jeden – mění se přístup k léčbě, můžeme cíleně inhibovat funkci přesně definované molekuly, konkrétní struktury či specifické buňky. Cílovými strukturami mohou být například regulátory metabolických a reparačních pochodů (cytokiny ze skupiny tumor‑necrosis factor, interleukinů, řady dalších růstových faktorů, např. v osteologii sklerostinu či aktivátoru [ligandu] receptoru NF‑κB – RANKL), nebo mohou být cílem enzymy, receptory, transportéry, iontové kanály, somatické buňky či bakteriální či virové antigeny. Specifickou oblastí je cílení efektu na podané léčivo, monoklonální protilátka pak působí jako antidotum. Novinkou je zavádění bispecifických monoklonálních protilátek vážících k sobě dvě molekuly – např. při léčbě hemofilie typu A s inhibicí faktoru VIII se užívá emicizumab vážící k sobě koagulační faktory X a IX, a suplující tak funkci faktoru VIII. Jak je vidět, možnosti biologické léčby, při obrovské plasticitě účinku, jsou nevyčerpatelné. Právě přesný zásah do cílové struktury (antigenu) s ovlivněním právě jen tohoto jednoho cíle je hlavní předností léčby. Pochopitelně však, pokud daný antigen na povrchu buňky není přítomen (např. při velké dediferenciaci tumorózní buňky), léčba se míjí účinkem.
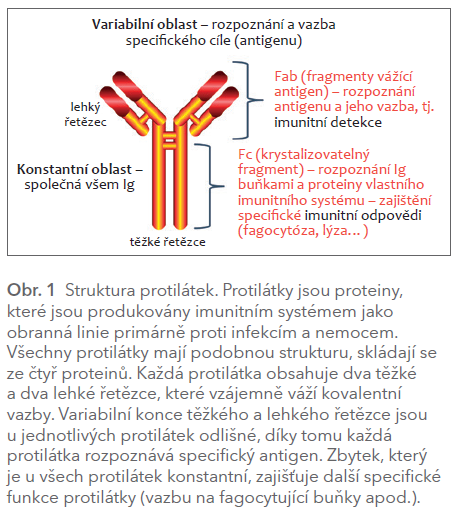
Imunoglobuliny (Ig) jsou produkovány B‑buňkami (plasmocyty) jako imunitní odpověď na různé noxy. V krvi pak buď cirkulují, či jsou vázané na membránu. Z pěti skupin imunoglobulinů se terapeuticky využívají jako monoklonální protilátky pouze IgG, které tvoří 80 % všech cirkulujících protilátek. Právě imunoglobuliny G zajišťují odpověď přesně cílenou na danou noxu v tzv. „druhé fázi“ odpovědi organismu. Výhodou protilátek typu IgG je také delší doba jejich cirkulace v organismu, pokud nedojde k navázání na antigen, jejich plazmatický poločas se pohybuje kolem 2–3 týdnů. Stavba všech imunoglobulinů je obdobná, základní strukturu tvoří dva těžké řetězce (≈400 aminokyselin) a dva lehké řetězce (110 aminokyselin) vzájemně spojené kovalentními vazbami (obr. 1). Po funkční stránce je důležitější rozdělení na variabilní oblast, sloužící k rozpoznání a k vazbě antigenu, a konstantní oblast, která je odpovědná za vazbu k Fc receptorům fagocytujících buněk, za vazbu komplementu, za rozpoznání vlastními imunocyty či za přenos imunoglobulinu např. placentární bariérou. Variabilní část je specifická pro každou buněčnou linii a váže se na specifické místo antigenu – epitop. Jeden antigen pak mívá epitopů několik a je terčem imunoglobulinů pocházejících z více plasmocytů. Pocházejí‑li protilátky z více buněčných linií, mluvíme o polyklonálních protilátkách, naopak jedna linie je zdrojem protilátek monoklonálních. Konstantní část je společná všem imunoglobulinům dané třídy.
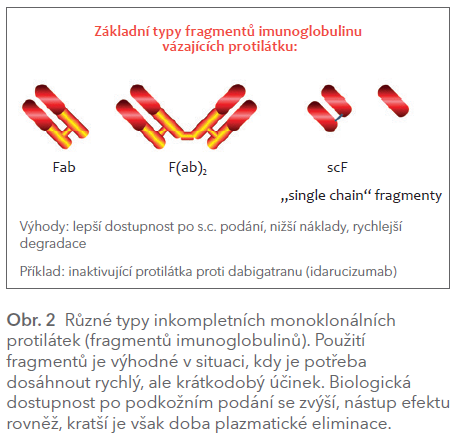
Kompletní protilátky a fragmenty komplexu. Léčebně využíváme imunoglobuliny buď kompletní – tvořené všemi čtyřmi řetězci, či aplikujeme jen jejich fragmenty (Fab), např. monomery či dimery variabilní části řetězce (obr. 2). Kompletní protilátky setrvávají v cirkulaci déle a lépe zajišťují likvidaci antigenu. Fragmenty pak mají při podkožním podání lepší dostupnost, rychleji jsou degradovány a mají menší výrobní náklady. V situacích, kdy potřebujeme rychlý a krátkodobý efekt – např. u protilátek typu antidota dabigatranu (idarucizumabu) – mohou být fragmenty výhodnější. Výhodnou modifikací jsou bispecifické fragmenty mAb, kdy jsou vázány dvě variabilní oblasti – jeden se specifitou např. k CD3 antigenu cytotoxické T‑buňky a druhý k antigenu na povrchu buňky určené k eliminaci. Cíleně tak mohou být ničeny např. tumorózní buňky.
Vývoj monoklonálních protilátek proběhl ve čtyřech generacích – od plně myších (ev. jiného nehumánního druhu) přes kombinované myší a lidské – tzv. chimérické s asi 30% podílem myšího Ig, či humanizované s pouze 5–10% podílem nehumánního antigenu až po plně lidské imunoglobuliny (obr. 3). Jednotlivé generace se významně liší zejména antigenicitou, která vzestupně klesá, či délkou účinku, která se prodlužuje. Trendem je užívání humánních monoklonálních protilátek.
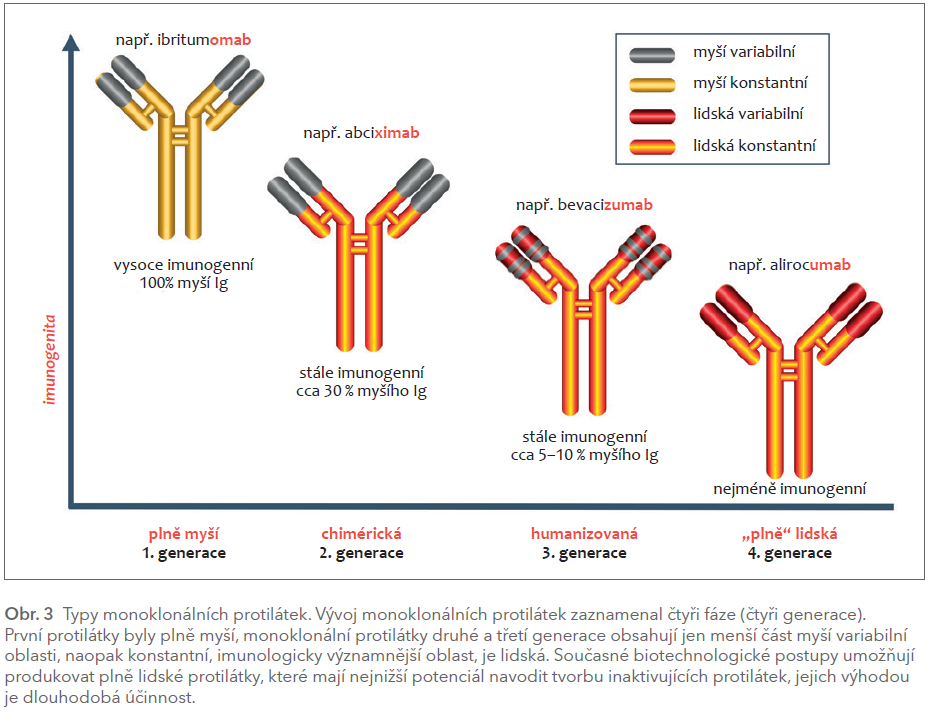
Názvosloví je odvozeno od jednotlivých generací monoklonálních protilátek (monoclonal antibody), tedy mAb: koncovka je vždy stejná ‑mab, další specifikace předchozím písmenem určuje, o jaký typ se jedná. Konkrétně ‑u‑ je rezervováno pro mAb humánní (např. alirocumab), ‑zu‑ pro humanizovanou, tedy kombinovanou s převahou lidské (např. idarucizumab), ‑xi‑ pro chimérickou s menším podílem lidské protilátky (např. abciximab) a ‑o‑ pro myší imunoglobulin. Čím větší podíl protilátek lidských, tím menší výskyt neutralizačních protilátek, které snižují výsledný efekt. Zejména pro dlouhodobou léčbu jsou optimální protilátky čistě lidské.
2. Farmakologické vlastnosti monoklonálních protilátek
Vzhledem k tomu, že – na rozdíl od „klasických“ léčiv s malými molekulami – jsou mAb tvořeny makromolekulou bílkoviny, farmakokinetické vlastnosti se u obou skupin významně liší (tab. 1).
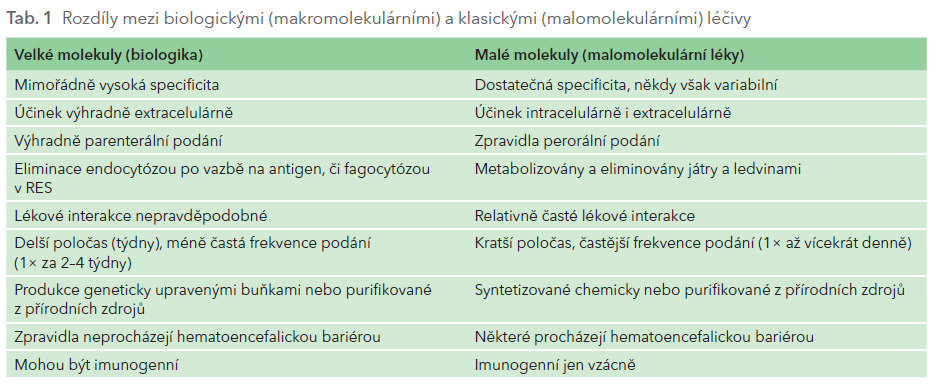
Aplikace je nutná zpravidla parenterálně. Nitrožilní podání má výhodu plné biologické dostupnosti a aplikace velkého množství léčiva. Naopak je zatíženo vyšším rizikem generalizované alergické reakce a je méně schůdné pro domácí léčbu. Podkožní podání je omezeno nižší biologickou dostupností pohybující se mezi 25–95 %, lépe jsou absorbovány fragmenty protilátek, naopak neocenitelnou výhodou je možnost domácí autoaplikace a výhodou je i větší bezpečnost.
Eliminace monoklonálních protilátek je dvojího typu. Prvým je eliminace zprostředkovaná cílovou strukturou (antigenem), kdy po vazbě protilátky a antigenu dochází k eliminaci komplexu např. fagocytózou následovanou lyzosomální degradací. Druhý typ, který není závislý na přítomnosti antigenu, využívá postupnou eliminaci buňkami RES. Na delším setrvání humánních Ig v cirkulaci se podílí vazba na Fc receptor na povrchu buněk, která je chrání před rychlou eliminací.
Toxicita monoklonálních protilátek jako takových je nevelká, alergické reakce u humánních či humanizovaných protilátek jsou při srovnání s placebem málo časté. V malém procentu se objevují lokální reakce typu pruritu, exantému apod. Daleko významnější jsou nežádoucí účinky vyplývající z farmakodynamického účinku, např. inhibice daného regulačního působku. Příkladem jsou protilátky proti TNFα či proti interleukinům, kdy je tangována obranyschopnost organismu. Vzhledem k tomu, že do farmakokinetiky mAb nejsou zapojeny transportní ani metabolické systémy, je riziko lékových interakcí nízké.
3. Příklady mechanismů působení monoklonálních protilátek v jednotlivých indikacích
Použití monoklonálních protilátek v onkologii má dlouhou tradici. Dominuje užití monotopických protilátek, kdy se obě vazebná ramena váží na povrchové epitopy konkrétních nádorových antigenů, růstových faktorů či např. vazoadhezivních proteinů. Vazba monoklonální protilátky na povrchový antigen nádorové buňky pak usnadní rozpoznání buňky obranným protinádorovým systémem. Vedle přímé likvidace buňky bývá zvýšena též účinnost cytostatik.
Vlastní protilátky mohou být cíleny proti membránovým antigenům lymfocytů, tak působí např. rituximab. Protilátka se váže na antigen CD20 s následnou indukcí apoptózy a cytolýzy. Jiné protilátky jsou cíleny proti dalším povrchovým antigenům, receptorům či interleukinům. Jiným mechanismem působení je snížení novotvorby tepenného zásobení nádoru, např. s užitím protilátky proti vaskulárnímu endoteliálnímu růstovému faktoru (VEGF) s cílem omezení růstu a metastazování. Příkladem je bevacizumab. Třetím příkladem jsou imunomodulační protilátky, které regulují imunitní odpověď.
Vedle těchto monotopických protilátek se zavádějí „konjugované“ protilátky, které se váží na epitopy nádorových buněk a současně s sebou nesou radionuklid či cytostatikum. Tak je zajištěna výrazně větší specificita účinku. Další možností je užití bispecifických, či dokonce trispecifických protilátek, které se na jedné straně váží na povrch nádoru, na straně druhé na T‑lymfocyt, který nádorovou buňku likviduje.
V gastroenterologii užíváme monoklonální protilátky k léčbě zánětlivých střevních onemocnění (IBD). Léčba je zamířena zejména k vyvázání klíčových mediátorů zánětu – užívají se především protilátky inaktivující tumor‑nekrotizující faktor alfa (TNFα) či jiné cytokiny (např. interleukiny podílející se v řetězci na uvolnění C‑reaktivního proteinu či vazoadhezivní molekuly umožňující transmukózní průnik buněk účastnících se zánětu).
Blokáda TNFα monoklonálními protilátkami (např. adalimumabem) vede k útlumu odpovědi organismu na cizorodé noxy, zejména však je potlačena imunitní odpověď. Přerušení významného článku v řetězci potlačí nadměrně vystupňovanou zánětlivou odpověď v rámci IBD, nejde však o léčbu kauzální. Jinou strategií je užití monoklonálních protilátek proti adhezivním molekulám (integrinům) na leukocytárním povrchovém receptoru. Tím je omezen průnik leukocytů do subendoteliálních prostor, při užití vedolizumabu je pak účinek selektivně omezen na střevo.
Další velkou oblastí, kde se užívají monoklonální protilátky, je revmatologie. Při systémových onemocněních pojiva hrají důležitou roli B‑lymfocyty a jejich interakce s T‑lymfocyty. Protilátky blokující lymfocytární antigen CD20 (např. již zmíněný rituximab) se vedle hemato‑onkologie užívá také v revmatologii k léčbě revmatoidní artritidy, vaskulitid a dalších jednotek. Jiná protilátka (belimumab) působí rovněž na úrovni B‑lymfocytů, je však cílena na inhibici stimulátoru těchto buněk (BLyS). V léčbě lupus erythematodes se využívá snížení hyperreaktivity právě B‑lymfocytů.
Biologická léčba je zavedena rovněž v neurologii, kde dominuje léčba roztroušené sklerózy. Alemtuzumab blokuje funkci antigenu CD52 exprimovaného lymfocyty T a B. Vazba protilátky na tento epitop vede k lýze lymfocytů. Podobně natalizumab je namířen proti adhezivní molekule (integrinu α‑4β‑1), a tím proti průniku lymfocytu do CNS. Třetím typem je užití ocrelizumabu namířeného proti leukocytárnímu antigenu CD20 s následným zabráněním poškození myelinové pochvy zánětem.
V pneumologii se užívají monoklonální protilátky v léčbě asthma bronchiale rezistentního na klasickou léčbu. Omalizumab inhibuje konstantní doménu FCε3 lidského IgE, a tak zabraňuje vazbě tohoto imunoglobulinu na buňky zprostředkující zánět (zejména mastocyty a eozinofily). Brání tak jejich degranulaci a uvolnění mediátorů alergické reakce, zejména histaminu.
Rovněž v kardiologii užíváme řadu monoklonálních protilátek. Abciximab se již desítky let užívá v rámci potlačení primární hemostázy. Vazba této protilátky na trombocytární receptory IIb/IIIa inhibuje agregaci. Některé monoklonální protilátky, zejména typu fragmentů, váží léčiva, a působí tak jako antidota (např. váží digoxin či dabigatran). Velmi perspektivní a již zavedené jsou protilátky proti regulátoru vychytávání lipoproteinu LDL v tkáních – proproteinové konvertáze subtilysin/kexinového typu 9 (PCSK9). Blokování funkce PCSK9 alirocumabem či evolocumabem zvýší expresi LDL‑receptoru a sníží koncentraci aterogenního LDL cholesterolu o 50–70 %.
Jak ukazuje tento (zdaleka ne vyčerpávající) přehled, biologická léčba se užívá v celé řadě oborů a průnik do dalších indikací nedá na sebe dlouho čekat. Zatím jediným faktorem omezujícím jejich ještě větší využití jsou vyšší náklady na léčbu. Praxe ukázala, že nutnost parenterální aplikace – jedná se o podávání jedenkrát za několik týdnů – není omezujícím faktorem, pacienti autoaplikaci dobře zvládají.
Léčba inhibujícími oligonukleotidy
Další – a zdá se velmi perspektivní – strategií, je cílená léčba inhibující tvorbu specifických proteinů přímo na úrovni genové translace genetické informace. Oligonukleotidy typu microRNA (miRNA) jsou řetězce malé nekódující RNA o délce 20–25 nukleotidů. Ty regulují expresi genů působením na messenger RNA – její degradaci, či vyřazením aktivity („silence”), proto se někdy označují jako siRNA. Ovlivněna je tak aktivita genů kontrolujících plejádu biologických dějů. Hlavním rozdílem proti biologické léčbě na bázi monoklonálních protilátek je zamezení syntéze proteinu, nikoli jeho inaktivaci.
Velmi slibným přístupem je užití chemicky modifikovaných, a proto i stabilních oligonukleotidů v léčbě metabolických (např. dyslipidemie), autoimunitních a neurologických (např. roztroušená skleróza), revmatických (např. revmatoidní artritida), infekčních (např. virus hepatitidy B) či nádorových chorob (např. hepatocelulární karcinom či glioblastom). V některých oblastech, např. v léčbě dyslipidemie, jsou některé miRNA schváleny k užití či jsou v poslední fázi klinického hodnocení.
Příkladem užití miRNA je léčba dyslipidemií. Jak bylo již řečeno, koncentrace lipoproteinu typu LDL a předávání cholesterolu do tkání jsou kontrolovány PCSK9. Volná konvertáza v plazmě vede k degradaci LDL‑receptoru a koncentrace aterogenních lipidů stoupá. Zavedena je inaktivace PCSK9 monoklonální protilátkou, prověřována je účinnost perorálně působících inhibitorů PCSK9. Druhou možností je užití inclisiranu, interferujícího oligonukleotidu (siRNA) inhibujícího translaci messenger RNA, a blokujícího tak funkci genu pro PCSK9. Pokles koncentrace konvertázy PCSK9 a LDL cholesterolu trvá po jedné aplikaci 6–12 měsíců.
Jiným příkladem je nová strategie léčby výrazně aterogenního a trombogenního lipoproteinu Lp(a). Zvýšená koncentrace výrazně zvyšuje riziko aterotrombotické příhody, dosavadní hypolipidemika snižují Lp(a) jen málo. Pelacarsen (AKCEA‑APO(a)LRX) je oligonukleotid inaktivující gen pro syntézu apolipoproteinu(a) vazbou na messenger RNA v hepatocytu. Pokles koncentrace Lp(a) o 30–80 % vede k normalizaci koncentrace téměř u všech nemocných. Vliv obou oligonukleotidů na pokles aterotrombotických příhod je prověřován v rámci třetí fáze klinického hodnocení.
Závěr
Lze konstatovat, že rozkvět farmakologie cílené na konkrétní molekulu s použitím nikoli chemických látek, ale léčiv na zcela novém biologickém podkladě, je teprve před námi. Respektive jsme již na prahu. Nepochybně pak přijdou další a další strategie – účinnější i bezpečnější. A bohužel, pravděpodobně i nákladnější.
Literatura
1. Chiu ML, Goulet DR, Teplyakov A, Gilliland GL. Antibody structure and function: The basis for engineering therapeutics. Antibodies (Basel) 2019;8:55.
2. Lu RM, Hwang YC, Liu IJ, et l. Development of therapeutic antibodies for the treatment of diseases. J Biomed Sci 2020;27:1.
3. Runcie K, Budman DR, John V, Seetharamu N. Bi‑specific and tri‑specific antibodies – the next big thing in solid tumor therapeutics. Mol Med 2018;24:50.
4. Saeed AF, Wang R, Ling S, Wang S. Antibody engineering for pursuing a healthier future. Front Microbiol 2017;8:495.
5. Shepard HM, Phillips GL, Thanos DC, Feldmann M. Developments in therapy with monoclonal antibodies and related proteins. Clin Med (Lond) 2017;17:220–232.
6. Ozcan G, Ozpolat B, Coleman RL, et al. Preclinical and clinical development of siRNA‑based therapeutics. Adv Drug Deliv Rev 2015;87:108–119.
7. Bajan S, Hutvagner G. RNA‑based therapeutics: From antisense oligonucleotides to miRNAs. Cells 2020;9:137.
zpět

